【令和版 パーキンソン病の症状14選】診断、予後って?歩行訓練で後ろ歩きは効果あるの?


パーキンソン病の臨床解剖学
パーキンソン病は、主に大脳基底核の障害と考えられています。
画像引用元:
How may the basal ganglia contribute to auditory categorization and speech perception?August 2014.Frontiers in Neuroscience 8(230):230
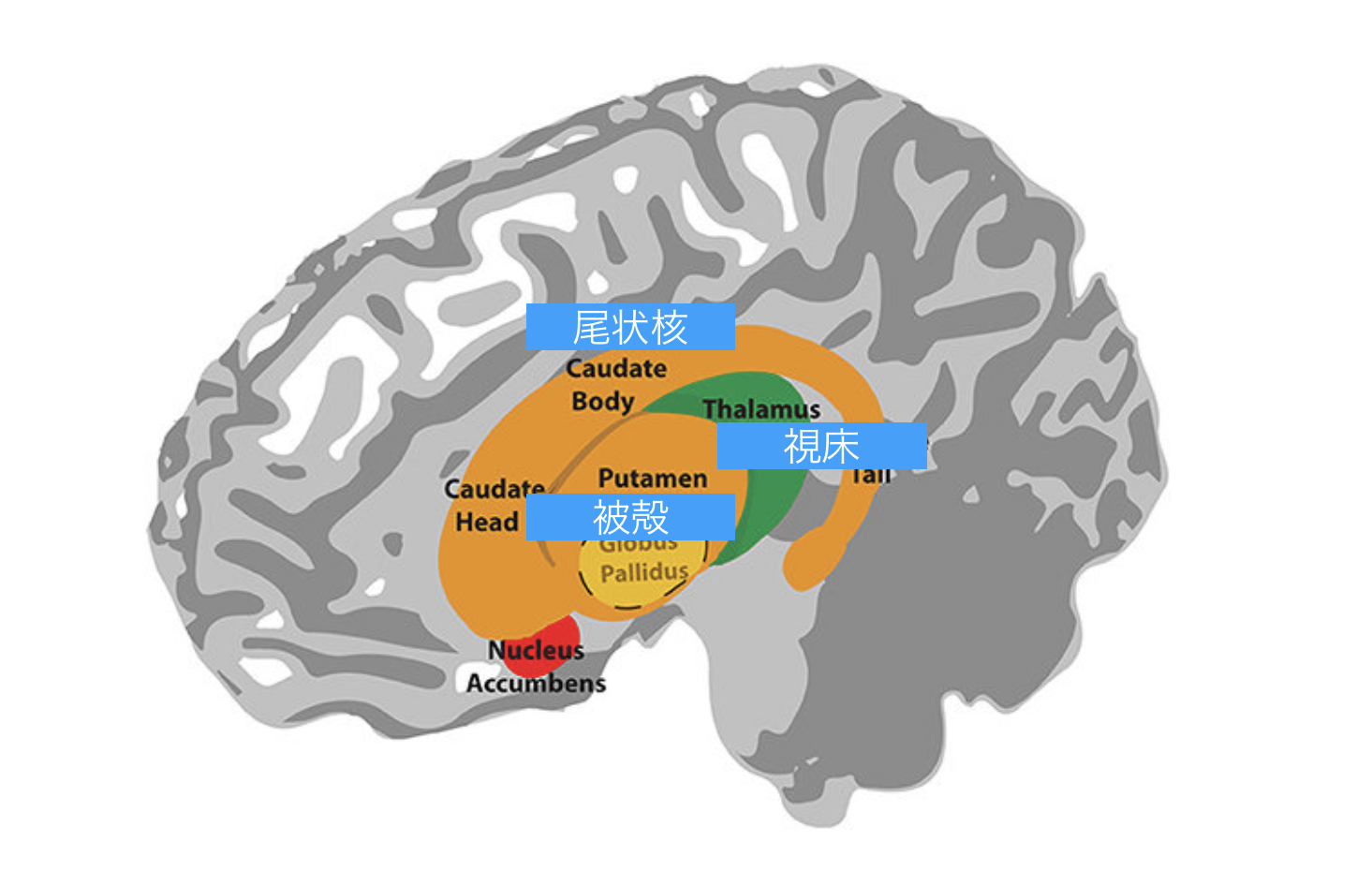
大脳基底核は、前脳の深部および中心部に位置する神経核の集まりであり、大脳皮質や視床、その他の部位と強固に結合しています。その膨大な情報伝達システムにより、自動的・随意的な運動制御、日常的な行動に関する手続き的学習、情動機能など、多くの機能に関与しています。他の皮質領域との連携により、運動制御や運動行動が円滑に実行されるようになります。
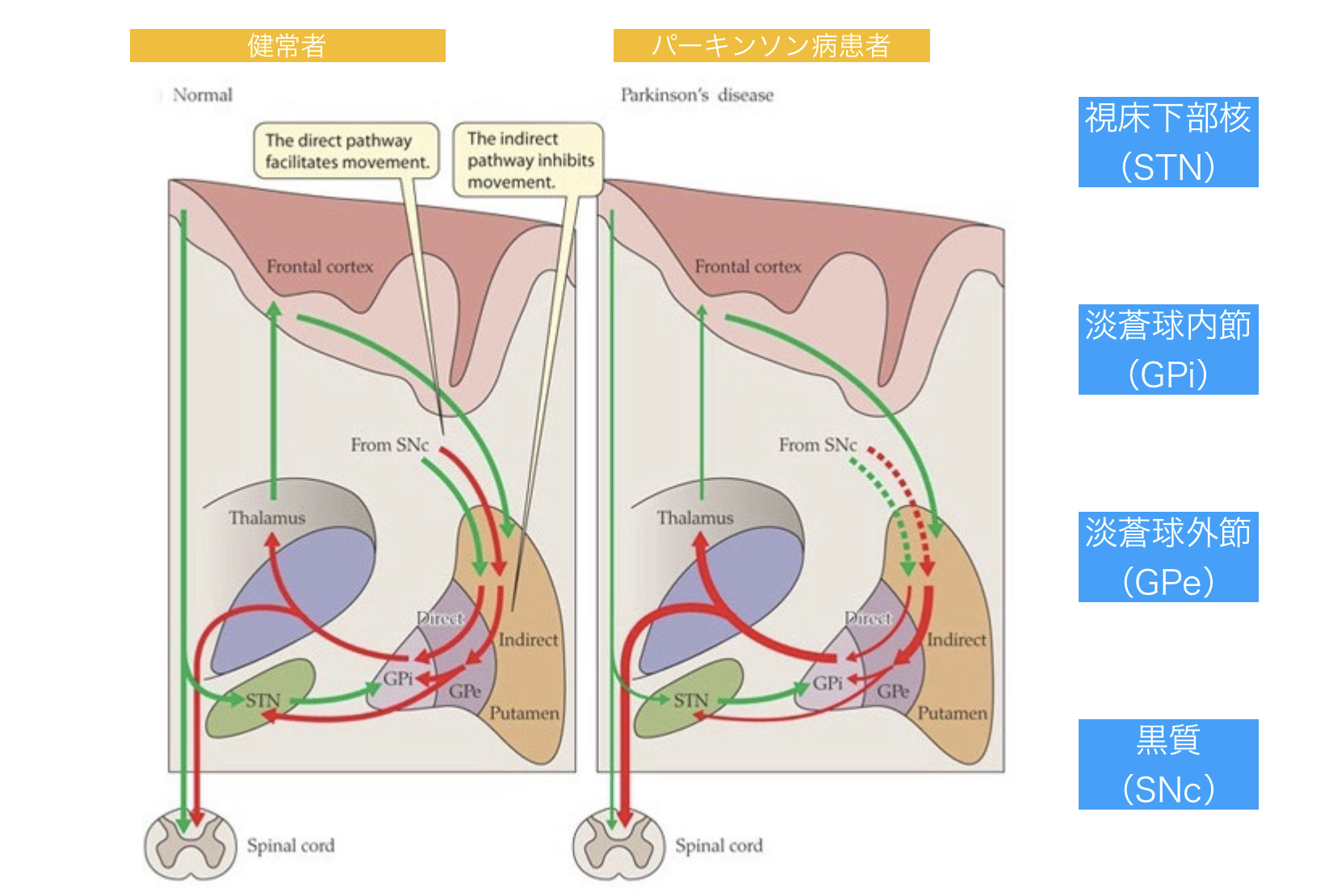
線条体は、大脳基底核の中で最も大きな核複合体であり、尾状核と被殻で構成されています。線条体は、大脳皮質の一部から興奮性の入力を受け、同時に黒質(SNc)のドーパミン作動性細胞から抑制性および興奮性の入力を受けます。これらの皮質および黒質からの入力は、2つのタイプの有棘の投射ニューロンによって受け取られます。
大脳基底核の主要な出力部位である淡蒼球内節(GPi)に直接投射するものです。すなわち、運動皮質が発火率を高めると、皮質脊髄路の活動が高まり、最終的には筋肉の活動も高まるので、運動システムの作用が「高まる」のです。
また、視床下核(STN)を介してGPiに至る間接的な経路を確立し、淡蒼球外節(GPe)に投射するものがあります。この間接経路の結果、視床から大脳皮質への興奮性ドライブが減少することになる。視床ニューロンの抑制が強まることで、実質的に大脳皮質からの運動活性が「低下」します。
両経路の作用によりGPiからの神経出力が制御され、一次運動野と補足運動野に投射する視床核に緊張性抑制性入力がもたらされます。
引用元:https://scienceofparkinsons.com/dopamine/
パーキンソン病の病態
パーキンソン病の病因は未だ不明であり、末梢神経系由来か中枢神経系由来か、振動子ネットワークか、基底核ベースの病態生理か小脳・視床ベースの病態生理かなど、様々な仮説があります。
従来、パーキンソン病は、死後の病理検査でレビー小体やカテコールアミン作動性神経細胞の変性が見つかることで定義されていました。しかしながら、この病理学的な定義を使用することは、現実の生活には即していないため、問題があります。
パーキンソン病の人の脳で認められている神経病理学的所見は以下の2つです。
まずは黒質緻密部の色素性ドーパミン作動性ニューロンの損失です。ドーパミンニューロンの損失は、腹外側黒質で最も顕著に起こります。
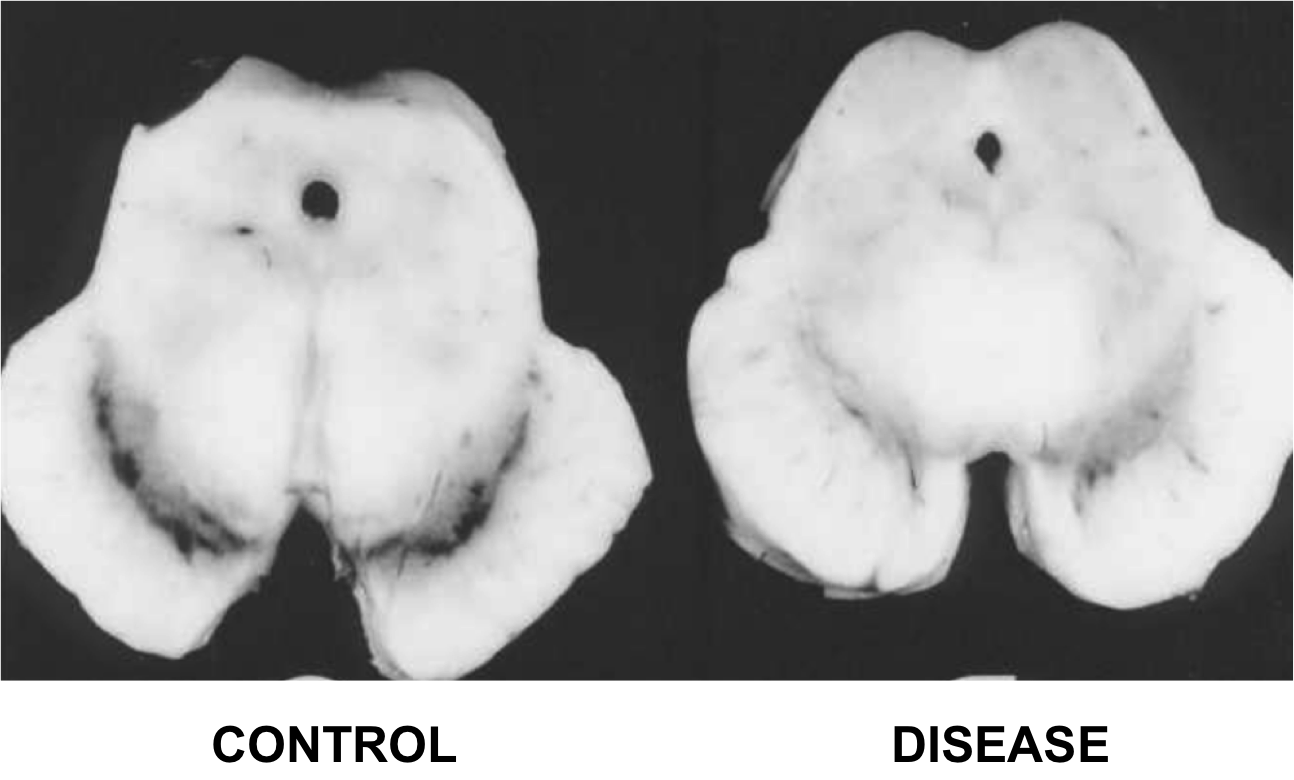
パーキンソン病の運動徴候が現れる前に、ドーパミン作動性ニューロンの約60~80%が失われます。ドーパミンの枯渇は、ドーパミンの黒質系の変性、抗精神病薬、化学物質に対する毒性反応または中毒から生じると考えられています。
次にレビー小体やレビー神経炎の存在です。死亡時に神経学的に正常と思われていた人が、剖検検査でレビー小体を有することが判明することがあります。これらの偶発的なレビー小体は、パーキンソンの症状発現前の段階であるという仮説が立てられています。その有病率は年齢とともに増加しますが、パーキンソン病に特異的で、非定型のパーキンソニズムや他の疾患の症例でも認められることがあります。
予後について
レボドパ以前
レボドパが導入される以前は、パーキンソン病は発症から5年以内に25%、10年以内に65%、15年以内に89%の患者に重度の障害または死亡をもたらしました。パーキンソン病による死亡率は、年齢、性別、人種をマッチさせた一般集団の3倍でした。
レボドパ後
レボドパの導入により、死亡率は約50%低下し、寿命は何年も延びました。これはレボドパの対症療法的な効果によるものと考えられており、レボドパが病気の進行性に起因しているという明確な証拠はありません。
予後に影響を与える要因
米国の神経学会では、以下の臨床的特徴がパーキンソン病の進行速度の予測に役立つと指摘しています。
発症時の年齢が高いこと、初期の固縮・運動低下により
(1)新たにパーキンソン病と診断された患者では運動機能の進行速度が速く
(2)認知機能低下や認知症の発症が早いこと
が予測できます。
しかし、最初に振戦を呈した場合は、病気の経過がより穏やかでレボドパによる治療効果が長くなることが予測できます。
患者が男性で、合併症があり、姿勢不安定/歩行困難(PIGD)がある場合にも、運動進行速度が速くなることが予測されます。
発症時の年齢が高いこと、認知症であること、ドパミン作動性治療への反応性が低下していることは、より早い老人ホームへの入居と生存率の低下を予測させる可能性があります。
パーキンソン病の診断方法
特発性パーキンソン病は、臨床的に3つのステージに分類されています。
1. 前臨床期:血液検査、唾液、遺伝子マーカーなどのバイオマーカーにより、病気の予知や早期発見が可能です。この段階では、危険因子を持つ人々を特定し、早期介入のためのトリアージを行うことができます。
2. 前駆症状期:この段階では、嗅覚の低下(低嗅覚)、気分の落ち込み、腸の症状、睡眠の変化などの症状が見られることが特徴です。
3. 症状発現期:ドパミン反応性運動機能、動作緩徐(大規模な感覚運動変化症状および疲労を伴う)、振戦および/または硬直によって定義される症状が見られることが特徴です。
パーキンソン病の診断には、その特徴の特異性と感度を明確に確立することが困難であるため、特定の標準的な基準は存在しません。病因は不明であり、ほとんどの場合、遺伝的要因と環境要因の組み合わせによるものと考えられています。ほとんどの人の場合、パーキンソン病の診断は臨床所見に基づいて行われます。
パーキンソン病の診断に最も広く受け入れられている臨床基準は、英国パーキンソン病協会ブレインバンクのパーキンソン病診断基準によって紹介されたものです。
ステップ1:パーキンソニズムの診断
動作緩徐と以下のうち少なくとも1つを示すもの
●筋硬直
●4~6Hzの安静時振戦
●一次的な視覚、前庭、小脳、固有感覚機能障害によらない姿勢不安定
パーキンソンの指標にはなるが、本来は診断基準ではない。他の多くの疾患による可能性もあります。
ステップ2:パーキンソニズムの原因として、パーキンソン病を除外する傾向がある特徴の一例
●パーキンソン病の症状が段階的に進行する脳卒中を繰り返した病歴
●度重なる頭部外傷の既往
●確定的な脳炎の病歴
●発症時に神経遮断薬による治療を受けている
●罹患した親族が1人以上
●持続的な寛解
●3年後に厳密に片側性であること
●小脳の徴候
●早期の重篤な自律神経障害
●記憶、言語、動作の障害を伴う初期の重度認知症
●バビンスキー徴候
●CTによる脳腫瘍または水頭症の存在
●レボドパの大量投与に否定的な反応
ステップ3:パーキンソン病の診断を裏付ける特徴(確定的なパーキンソン病と診断するためには3つ以上が必要です)
●片側のみの発症
●安静時振戦がある
●進行性の障害
●発症した側に最も影響を与える持続的な非対称性
●レボドパに対する反応性が良好(70-100%)
●重度のレボドパ誘発性コレア
●5年以上のレボドパ反応性
●10年以上の臨床経過
近年、パーキンソン病を遺伝的に定義する試みが、単遺伝子型の発見により可能になりました。現在知られているパーキンソン病の遺伝的原因は、症例の約10%を占めています。
診断におけるPET検査、MIBG心筋シンチグラフィーの役割
パーキンソン病のいくつかの症状の原因となる主要な化学物質であるドーパミンの喪失を検査することで、ドーパミンの欠乏がない人の検査と比較することができます。この検査は、パーキンソン病の診断を下すためのものではなく、ドーパミン作動性神経細胞の減少を特定するために使用されます。パーキンソン病の診断が不確かな場合、経験豊富な神経科医が使用します。
検査には、放射性核種を用いたポジトロン断層撮影法(PET)、または単一光子放射断層撮影(SPECT)と呼ばれる方法で、患者の静脈に放射性医薬品(脳内のドーパミントランスポーター(DaT)の存在を検出するために使用)を注入する方法が含まれます。
PET検査はグルコース(糖)代謝に、DaT/SPECT検査はドーパミントランスポーターの活性に着目した検査が一般的です。残念ながら、このような低下は、多系統萎縮症(MSA)や進行性核上性麻痺(PSP)など、パーキンソン病以外の疾患でも認められます。
パーキンソン病では、心臓交感神経の変性・脱神経がみられるため、心臓交感神経に集積する核種であるMIBGを投与して撮影するMIBGシンチグラフィ検査では、心臓における核種の集積低下がみられます。 パーキンソン病では80~90%で同所見がみられ、その他のパーキンソン症候群や本態性振との鑑別の一助になります。
パーキンソン病の正確な診断の価値
パーキンソン病が疑われる人の正確な診断は、特に若年発症の診断では、予後に重要な影響を及ぼします。パーキンソン病の患者は、MSAやPSPの患者よりも寿命が長く、ドパミン作用のある薬物療法によく反応するようになります。さらに、本態性振戦に見られるような姿勢振戦や動作振戦など、振戦を呈する他の疾患との鑑別が必要です。
パーキンソニズムやパーキンソン症候群の他の原因としては、多発性脳梗塞が挙げられます。また、高齢者では錐体外路症状や徴候がよくみられるため、鑑別診断が困難な場合があります。
パーキンソン病を予測する要因
Schragらによる2014年の研究では、パーキンソン病と診断される前に存在する運動および非運動症状を特定することを目的としています。
振戦、平衡障害、便秘、低血圧、勃起障害、排尿障害、めまい、疲労、うつ病および不安は対照群と比較して、パーキンソン病と診断される5年前の患者さんに高い割合で存在しました。
また、パーキンソン病の初期診断上の特徴のひとつとされる「便秘」は、診断の10年前に高率に認められることがわかりました。診断の2年前からは記憶障害の発生率が高いことが報告されています。
パーキンソン病の典型的症状 14選
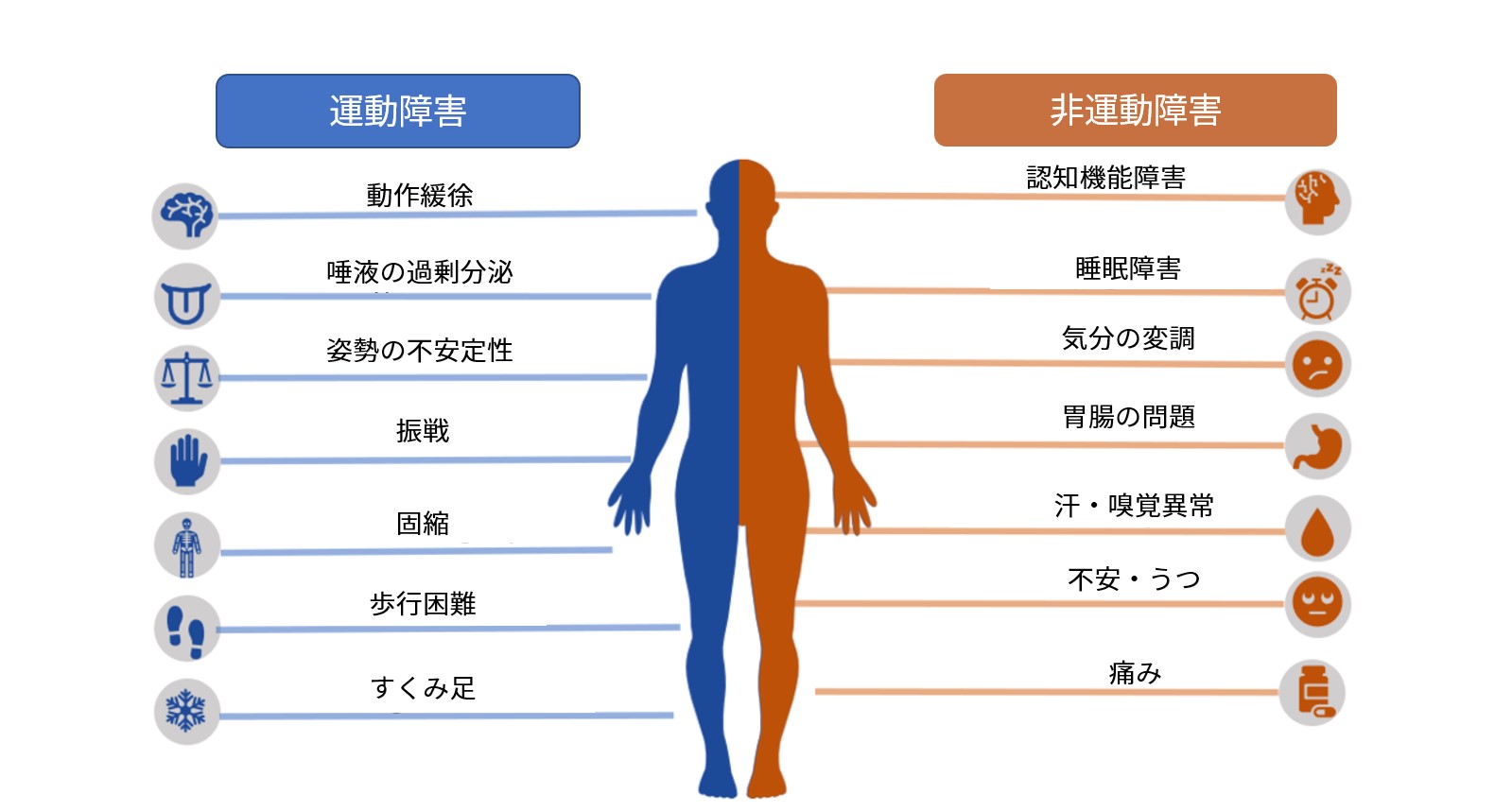
パーキンソン病の運動症状に関しては下記記事でまとめています。併せて勉強してみてください。

パーキンソン病に役立つ動画
カテゴリー
脳科学,パーキンソン病,歩行
タイトル
パーキンソン病における後歩きの研究 Backward walking in Parkinson’s disease?PubMedへ Hackney ME et al:Mov Disord. 2009 Jan 30;24(2):218-23
内 容
目 的
・台所の流しから離れたり、目の前を車が通ったりする時など、日常的に後ろ向きに歩くことがある。
・PD患者にとってこの後ろ歩きは難しい動きである。
・この研究は、対照群と比較して、軽度から中等度のPDを有する患者の後ろ歩きを評価することを目的とした。
方 法
・特発性PD(H&Y範囲:0.5〜3)、年齢および性別が一致した対照群の前歩きと後歩きを評価した。
・参加者は、 PD(平均年齢= 65.1±9.5歳、女性:28%)および74人の年齢および性別の対照(平均年齢= 65.0±10.0歳、女性:23%)の患者が参加した。参加者は、PD以外の神経学的欠損の病歴または証拠があれば除外した。
・UPDRSおよびバーグ・バランス・スケール(BBS)を用いて評価した。転倒群は、過去6ヶ月間に1回またはそれ以上の転倒を報告した人々であった。
・すくみ足は、歩数アンケートFreezing of Gait questionnaire (FOG) によって決定された。
・FOGの項目3でスコアが1以上の場合、すくみ足有するとみなされ、1週間に1回以上の頻度を示している。
・平均UPDRSモーターサブスケール3スコアは27.5±9.2であり、疾患を有する期間は8.2±5.0年であった。
・PDの患者の50%が転倒の既往歴があり、45%がすくみ足が出現する患者であった。 ・前後の歩行は、5mのコンピュータ管理された歩道を用いて測定された。
・各方向の試行の結果を平均した。
・対象となる主要な変数は、歩行速度、ストライド長、歩行率(ケイデンス)、BOS:ヒールからヒールの支持基盤(m)、両脚支持期(率)、遊脚および立脚(率)、および機能的歩行プロファイル(Functional Ambulation Profile)であった。
・FAP値は、歩容の変動性を定量化し、速度が脚の長さに正規化されたときのステップの長さ/脚の長さの比とステップ時間の線形関係を構成する。
結 果
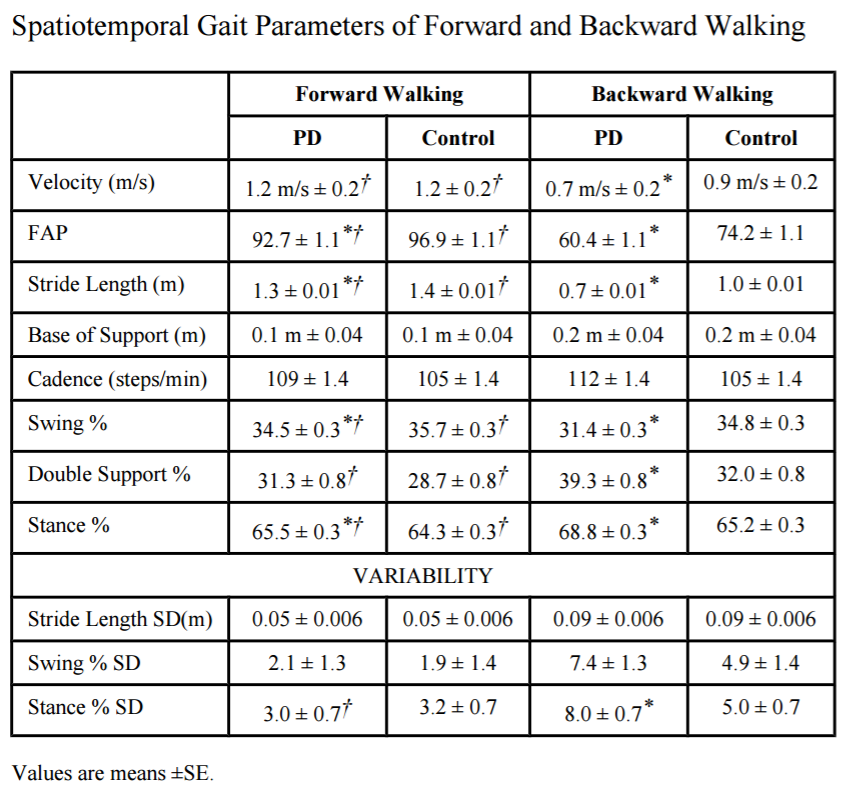 (Hackney ME et al:2009)?PubMedへ
(Hackney ME et al:2009)?PubMedへ
・Velocity-FW(前歩き)では、グループは同様の速度で歩き、両群ともBW(後ろ歩き)中にFWより有意に遅く歩いた。BWでは、PD患者は対照群よりも歩行速度が遅かった。
・Stride Length (m)-PD群では、FWおよびBWの対照群に比べ、有意に短いストライド長で、両群ともFWよりもBW時に有意に短いストライド長で歩いた。
・Swing % -PD群では、FWとBWの両方で対照群よりも遊脚期(率)が短く、両群ともFWと比較した場合、BWでのより短い遊脚期が認められた。
・Stance %-PD群では、FWおよびBWの対照群よりも立脚期の時間が長く、 両群ともFWと比較した場合、より長い立脚(率)がBWに認められた。
・Double Support %-BWでは、PDを有する患者は対照よりも大きい両脚支持率で歩行した。 PDおよび対照群の両方で、BW中の両脚支持率がFWよりも多かった。 ・Base of Support (m)-両群とも、FWよりもBW中に有意に広いBOSで歩行した。
・Cadence (steps/min) -PDを有する者は、対照よりも多い歩数で歩いた。
・FAP-PDを有する患者は、FWおよびBWの両方において、対照より有意に低いFAP値を有した。両群とも、FWよりBW中に有意に低いFAP値を示した。
・Variability of Gait Measures-対照およびPDを有する患者は、FWにおける類似の立脚の変動性を有していた。PDを有する患者は、対照よりもBWの立脚の変動性が大きかった。
・PDの患者では、立脚の変動性はBWがFWよりも大きかった。BWは、立脚、歩隔、遊脚において、FWよりも変動性があった。
・UPDRSはFW速度と無相関であった。 FW速度が増加するにつれて、BW速度は増加した。
・BBSスコアが上昇すると、BWとFWの両方の速度が増加した。PDとFWまたはBWの間に有意な関係は見られなかった。
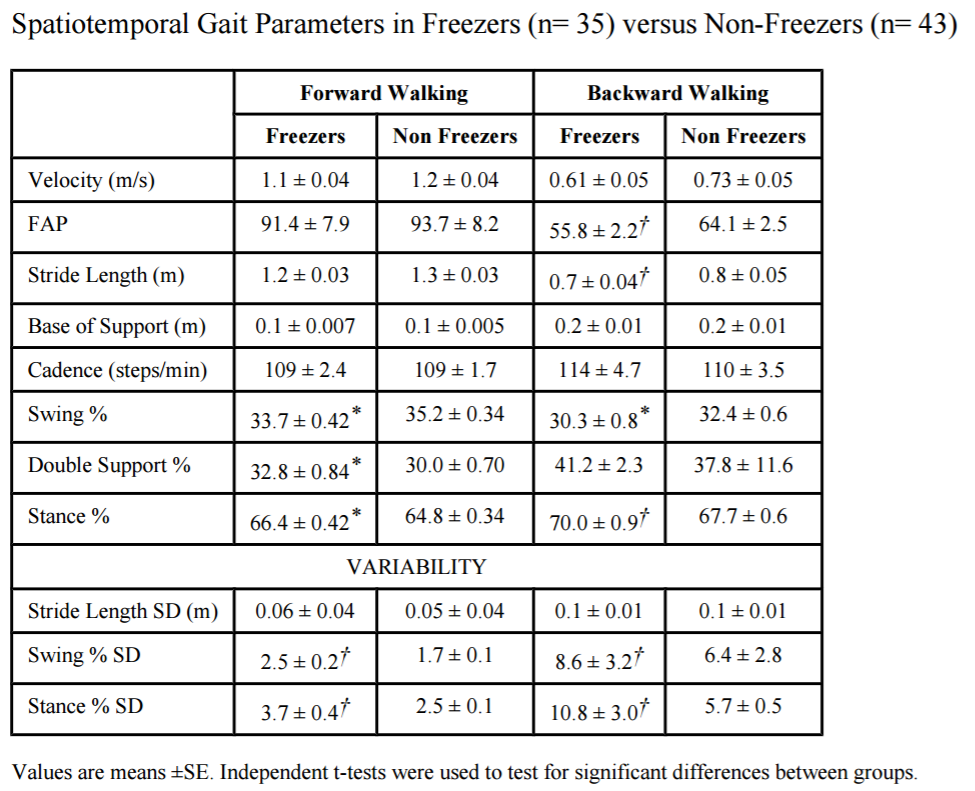 (Hackney ME et al:2009)?PubMedへ
(Hackney ME et al:2009)?PubMedへ
・上表は、すくみ足の有り/無しの結果をまとめたものである。 ・すくみ足有りの群は、無しの群より有意に短い遊脚(%)および長い両脚支持(%)および立脚(%)を有していた。ストライド長に関してはFW変動性において類似していた。すくみ足群は、立脚および遊脚においてより無しの群より変動的であった。
・BWでは、すくみ足有りの群は、無しの群より有意に低いFAPスコア、ストライド長、遊脚期(%)、およびかなり高い立脚(%)を有していた。歩隔はBW変動性において類似していた。すくみ足の群は、より立脚/遊脚共に変動性があった
まとめ
・後ろ歩きでは視覚的手がかり得られづらく、前歩きよりも固有感受性に大きく依存するため、後歩き中のストライドの長さを伸ばすことができなかったと思われる。
・PDにおける姿勢不安定性は、基底核における固有受容シグナルの異常処理に起因する固有感覚障害に関連している可能性がある。
・PDを患っている人は、特に横方向および後ろ方向に、摂動されると拮抗筋を過度に活性化する。
・PD薬物療法はそれを改善することはほとんどなく、PDにおける後方の不安定性はレボドパ耐性であり、視床下部の刺激によって助けられない。
・変動性は、対照群と比較してPD群の立脚(%)で最も明白であった。
・すくみ足群は、より長い病気期間を有し、よりバランスが損なわれ、すくみ足の無い群と比べやや劣る性能及びより大きな変動性が見られた。
・今回の研究でのPDグループは対照と同様の速度で歩いたが、ストライド長、遊脚および立脚(%)およびFAP値は、対照と比較してFWにおいて低下した。これは、歩行速度が事実上損なわれていないことを示す研究と一致しているが、FWの他の時空間的特徴は発症間もないPDでも影響を受ける。
・本研究は、PDを有する個体は、FWの低下を上回るBWの低下を有することを実証している。
・同様に、正常または軽度に障害のあるFWを有するPD患者は、ターン動作時により大きな障害を示す。Crennaらは、FW機構から分離され、PDの影響を受け易い神経系がターン動作を仲介する可能性が高いことを提案している。
・最近の研究がFWおよびBWのための別個の制御システムの存在を示唆している。 FWとBWが別々の神経システムによって制御される場合、これらのシステムはPDによって差異的に影響を受ける可能性がある。現在の研究は、病気の過程の早い段階で後方システムが影響を受ける可能性があることを示唆している。
・BW障害は後方転倒の傾向に関連している可能性があるため、BWの評価は重要な臨床的ツールとなりうる。
・BW観察は、FWよりも基底核が損なわれる程度をより具体的に示すことができる。
・BWはリハビリにて有用である可能性がある。実際には、多方向歩行と歩行訓練がPD患者の転倒の発生率と歩行の改善を減少させた。
・今後の研究では、BW対FWに対する二重課題のようなタスクの複雑性の増大や踏み台訓練上でのBWなどのリハビリの可能性を探る研究が必要である。
私見・明日への臨床アイデア
・PD患者における後ろ歩きの練習は日頃良く見かける光景である。BWは筋の使う場所だけでなく、固有感覚が優位になったり、FWとまた違った神経系を活性化することが窺える。しかし、視覚が使えない、普段行わないなどFWより難しい課題ともなり得、代償の反応も評価して用いるのであれば練習する必要があると思われる。
・パーキンソン病の姿勢変形に対する介入については下の記事でまとめています。
執筆監修|金子 唯史 STROKE LAB代表
・国家資格(作業療法士)取得
・順天堂大学医学部附属順天堂医院10年勤務
・海外で3年に渡り徒手研修修了
・医学書院「脳卒中の動作分析」など多数執筆
脳卒中の動作分析 一覧はこちら
塾講師陣が個別に合わせたリハビリでサポートします

1981 :長崎市生まれ 2003 :国家資格取得後(作業療法士)、高知県の近森リハビリテーション病院 入職 2005 :順天堂大学医学部附属順天堂医院 入職 2012~2014:イギリス(マンチェスター2回,ウェールズ1回)にてボバース上級講習会修了 2015 :約10年間勤務した順天堂医院を退職 2015 :都内文京区に自費リハビリ施設 ニューロリハビリ研究所「STROKE LAB」設立 脳卒中/脳梗塞、パーキンソン病などの神経疾患の方々のリハビリをサポート 2017: YouTube 「STROKE LAB公式チャンネル」「脳リハ.com」開設 現在計 9万人超え 2022~:株式会社STROKE LAB代表取締役に就任 【著書,翻訳書】 近代ボバース概念:ガイアブックス (2011) エビデンスに基づく脳卒中後の上肢と手のリハビリテーション:ガイアブックス (2014) エビデンスに基づく高齢者の作業療法:ガイアブックス (2014) 新 近代ボバース概念:ガイアブックス (2017) 脳卒中の動作分析:医学書院 (2018) 脳卒中の機能回復:医学書院 (2023) 脳の機能解剖とリハビリテーション:医学書院 (2024)
















